|
♦
Главная
♦
Самарская Лука
♦
Введение
♦
Источники
♦Фитодиагностика
♦
Святая вода
♦
Чаепитие
♦
Фитококтейли
♦
Сокодвижение
♦
Лечение водой
♦
Праздники воды
♦
Память воды
♦
Фото-выставка
♦
Выводы
♦
Авторы
♦
Литература
| |
Общие результаты

1.
К
работе над проектом привлечены около двухсот учащихся.
2.
Было проведено четыре 16-ти часовых экспедиции. В этих экспедициях приняли
участие 82 человека.
3.
Набран видео и фотоматериал, проанализирована вода семи источников. Измеряли
температуру воды источников. По каждому из них составили паспорт.
4.
Условились с местными жителями будущей весной приехать и оказать посильную
помощь в реконструкции часовни Саввы.
5.
Ведется поиск сподвижников для расчистки источника Космы и Дамиана.
6.
Приступили к созданию виртуальной эколого - краеведческой тропы для путешествия
по территории Самарской Луки для всех желающих (ведь Самарская Лука находится
далеко от города Самары, да и большая ее часть закрыта для праздного посещения
- Национальный парк и заповедник). Создали и выставили в Интернете сайт
http://www.kluchijigulgor.narod.ru
7.
Мы
вступили в ряды Друзей Национального Парка Самарская Лука.
8. В экспедициях мы
делали забор воды и
анализировали ее в школьной лаборатории
реактивами из химического рюкзачка. Всего было сделано 98 анализов собранной
воды.
Что же мы получили?
 1.
Показатели рН, наличие карбонатов,
фосфат- аниона, нитрит- аниона и железа значительно ниже ПДК, установленных
СанПином. 1.
Показатели рН, наличие карбонатов,
фосфат- аниона, нитрит- аниона и железа значительно ниже ПДК, установленных
СанПином.
2. Показатели хлорид- ионы и ОЖ в 1,5- 3
раза выше нормы. Это можно объяснить близостью к водоносным слоям залежей
карбонатов и хлоридов (доломиты, известняки, поваренная соль характерны для
Жигулевских гор). Подземные воды, как правило, имеют эти показатели значительно
выше норм для поверхностных вод, а именно с этим уровнем показателей мы ведем
сравнение, т.к. нас интересует в первую очередь родник, как источник воды
поверхностного использования - питание рек, растений, животных, человека.
3. По показателю катион - аммония пять из
семи источников имеют превышения:
- источник Космы и Дамиана
незначительно - на 0,31 мг/л. Это можно объяснить тем, что выход источника
покрыт слоем воды, местность вокруг заболоченная. Несмотря на достаточно
холодную воду (10 градусов), процесс разложения растений и погибших гидробионтов
происходит и повышает уровень данного показателя.
- источник Богородицы Всецарица - в 7
раз, Винный- в 14 раз. Эти источники расположены на территории населенных
пунктов. В их воду как-то могли попасть стоки жизнедеятельности человека.
- источники Богородицы и Николая Чудотворца имеют
превышение в 10 и 14 раз соответственно. Но они расположены далеко от населенных
пунктов и других объектов деятельности человека. Вероятно, превышение норм можно
объяснить близостью залегания нефтяных пластов. Впрочем, этим же можно объяснить
и предыдущие два случая.
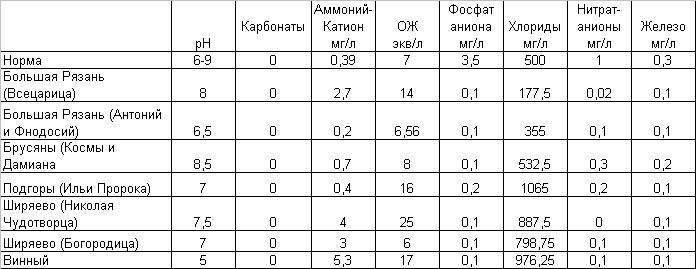
см.
диаграммы
Общие
выводы
1.
Жигулевские горы сложены пористыми породами, легко впитывающими воду. Поэтому в
Жигулях мало источников, все они известны человеку, многие почитаются как святые.
2. Шесть из семи источников не доносят воду до ближайшей реки Волги. Значит, не
оказывают непосредственного влияния на характеристики речной воды. Два участвуют
в образовании болот с их специфическими особенностями и значением. Четыре
источника питают водой окружающую их жизнь. Вода шести источников используется
для человеком для питья и в целебных целях, например, закаливающее обливание.
3. На химический состав воды оказывают влияние характерные для Жигулевских гор
породы: карбонаты, хлориды, нефтяные пласты.
4. По химическому составу воды (исследуемых нами показателей) святые источники не
отличаются от вод обычных, неосвященных источников.
Справка.
|
Хлориды
присутствуют практически во всех водах. В основном их присутствие в воде
связано с вымыванием из горных пород наиболее распространённой на Земле
соли – хлорида натрия (поваренной соли). Повышенное содержание хлоридов
в совокупности с присутствием в воде аммиака, нитритов и нитратов может
свидетельствовать о загрязнённости бытовыми сточными водами.
ПДК хлоридов в воде питьевого качества – 300…350 мг/л (в зависимости от
стандарта).
Железо
может встречаться в природных водах в следующих видах:
• Истинно растворённом виде (двухвалентное железо, прозрачная бесцветная
вода)
• Нерастворённом виде (трёхвалентное железо, прозрачная вода с
коричневато-бурым осадком или ярко выраженными хлопьями)
• Коллоидном состоянии (окрашенная желтовато-коричневая опалесцирующая
вода, осадок не выпадает даже при длительном отстаивании)
• Железоорганика – соли железа и гуминовых и фульвокислот (прозрачная
желтовато-коричневая вода)
• Железобактерии (коричневая слизь на водопроводных трубах)
Аммоний-ион
(NH4+).
В природных водах накапливается при
растворении в воде газа аммиака (NН3), образующегося при
биохимическом распаде азотсодержащих органических соединений.
Растворенный аммиак (аммоний-ион) поступает в водоем с поверхностным и
подземным стоком, атмосферными осадками, а также со сточными водами
промышленных предприятий. В поверхностных водах, насыщенных кислородом,
под действием нитрифицирующих бактерий быстро окисляется до неустойчивой
нитритной (N02-),
а затем - до устойчивой нитратной (N03-),
формы. Наличие аммоний-иона в концентрациях, превышающих фоновые
значения, указывает на свежее загрязнение и близость источника
загрязнения (коммунальные очистные сооружения, отстойники промышленных
отходов, животноводческие фермы, скопления навоза, азотных удобрений,
поселения и турбазы).
В природных водах встречается в очень незначительных
концентрациях, зачастую недоступных существующим массовым методам
анализа (сотые доли мг/дмЗ).
Увеличение концентрации ионов аммония и
аммиака может наблюдаться в осенне-зимние периоды отмирания водных
организмов, особенно в зонах их скопления. Уменьшение концентрации этих
веществ происходит весной и летом в результате интенсивного их усвоения
растениями при фотосинтезе. Прогрессирующее повышение концентрации
аммоний-иона в воде указывает на ухудшение санитарного состояния
водоема.
Общая
сумма карбонатной и некарбонатной жесткости.
Вода поверхностных источников, как правило, относительно мягкая (3…6
мг-экв/л) и зависит от географического положения – чем южнее, тем
жесткость воды выше. Жесткость подземных вод зависит от глубины и
расположения горизонта водоносного слоя и годового объема осадков.
Жесткость воды из слоёв известняка составляет обычно 6 мг-экв/л и выше.
По СанПиНу 2.1.4.559-96 жесткость питьевой воды должна быть не выше 7,0
мг-экв/л
Жесткость воды
определяется содержанием в воде солей жесткости (кальция и магния). Она
выражается в миллиграмм-эквивалентах на литр (мг-экв/л). Различают
следующие виды жесткости:
Карбонатная – характеризуется содержанием в воде гидрокарбоната кальция,
который при кипячении разлагается на практически нерастворимый карбонат
и углекислый газ. Поэтому её еще называют временной жесткостью.
pH воды - один из важнейших показателей
качества воды. Он во многом определяет характер химических и
биологических процессов, происходящих в ней. В зависимости от величины
pH может изменяться скорость протекания
химических реакций, степень коррозионной агрессивности воды, токсичность
загрязняющих веществ и т.д. Обычно уровень pH
в речных водах находится в пределах 6,5-8,5, в атмосферных осадках -
4,6-6,1, в болотах - 7,9-8,3. А вот для питьевой и
хозяйственно-бытовой воды самый оптимальный уровень - 6-8. Но все-таки
для питьевой воды лучшее число - 7. |
Назад
| |
|
